 |
 |

Bisphénol A et Risque de Désordres Métaboliques
Frederick S. vom Saal, PhD;
John Peterson Myers, PhD
JAMA. 2008;300(11):1353-1355
Dans ce numéro de JAMA, LANG ET AL.1 rapportent les résultats de la première étude épidémiologique majeure pour examiner les problèmes de santé liés au composant chimique oestrogénique omniprésent bisphénol A (BPA). Ce composant est la base chimique (monomère) utilisée pour fabriquer des contenants en plastique de type polycarbonate pour les boissons et la nourriture, le revêtement résine intérieur des conserves, et les prothèses dentaires ; on le trouve également dans le papier « sans carbone » utilisé pour les reçus aussi bien que dans une gamme étendue d’autres articles ménagers communs. Basé sur leur analyse de données de l’Enquête 2003-2004 d’Examen de Santé et de Nutrition National, Lang et al. rapportent une relation significative entre les concentrations dans l’urine de BPA et une maladie cardiovasculaire, un diabète de type 2, et des anomalies d’enzymes du foie dans un échantillon représentatif de la population américaine adulte. Ce rapport, suggérant des liens entre le BPA et certaines maladies les plus significativement et économiquement onéreuses, est basé sur une étude transversale et par conséquent ne peuvent établir de causalité ; des études longitudinales de suivi devraient en conséquence être une priorité. Cependant de nombreuses études passées en revue par des pairs rapportent des effets secondaires du BPA sur des animaux expérimentaux 2 et des études de cellules identifient les mécanismes moléculaires qui influencent ces réponses.3 Ces découvertes expérimentales ajoutent une plausibilité biologique aux résultats apportés par Lang et al.1
En se basant sur cette information de contexte, l’étude de Lang et al.,1 pendant le préliminaire en ce qui concerne ces maladies chez l’homme, devrait stimuler les agences américaines pour suivre l’action récente entreprise par les agences de régulation du Canada, qui avaient déclaré le BPA « toxique chimique » nécessitant une action agressive pour limiter les expositions humaine et environnementale.4 Alternativement, une action du Congrès pourrait suivre l’ensemble précédent avec le passage récent de la législation fédérale conçue pour limiter les expositions à une autre famille de composés, les phtalates, également utilisés dans le plastique. Comme le BPA,5 les phtalates sont détectables chez virtuellement tout le monde aux Etats-Unis.6 Cette loi rapproche la politique américaine du modèle européen, dans lequel l’industrie doit fournir des données sur la sécurité d’un composé chimique avant qu’il puisse être utilisé dans les produits.
Après une observation inopinée de 1997, de nombreuses études sur des animaux de laboratoire2 ont identifié des effets semblables à ceux de drogues à faible dose du BPA à des niveaux inférieurs à la dose utilisée par la Food and Drug Administration (FDA) et l’Agence de Protection de l’Environnement pour estimer la dose de prise journalière humaine courante acceptable (DJA) considérée comme sûre pour l’homme. Ces études ont montré des effets secondaires du BPA sur le cerveau, le système de reproduction, et – plus pertinent pour les découvertes de Lang et al.1 – les processus métaboliques, y compris des altérations de l’hémostase de l’insuline et les enzymes hépatiques.2 Cependant, aucune étude antérieure examinant le BPA pour ses effets sur la fonction cardiovasculaire n’a été menée sur des animaux de laboratoire ou chez l’homme.
Les épidémiologistes sont informés par des études sur les animaux qu’identifier les problèmes de santé potentiels humains lorsque les modèles animaux et les niveaux d’exposition sont pertinents et les effets sont influencés par les mécanismes de réponse présents chez l’homme. Par exemple, lorsque des rats adultes étaient nourris avec 0,2-µg/kg par jour de BPA pendant 1 mois (une dose 250 fois inférieure à la DJA habituelle), le BPA diminuait significativement les activités des enzymes antioxydants et augmentaient la peroxydation lipidique, augmentant ainsi le stress oxydatif.7 Lorsqu’on a administré à des souris adultes une dose de BPA de 10- µg/kg par jour pendant 2 jours (une dose 5 fois inférieure à la DJA), le BPA stimulait les cellules pancréatiques β pour produire de l’insuline. Après administration de 100- µg/kg par jour de BPA par injection ou alimentation pendant 4 jours, les souris développèrent une résistance à l’insuline et une hyperinsulinémie postprandiale. Des études de suivi ont montré que la stimulation de la production et de la sécrétion chez la souris des cellules β de l’insuline par l’oestradiol entre 0,1 et 1nM ou du BPA (23-230 pg/mL de BPA) est influencée par l’activation de la protéine kinase extracellulaire liée au signal 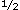 chemin par liaison du BPA au récepteur d’oestrogène chemin par liaison du BPA au récepteur d’oestrogène  et que par ce mécanisme non classique de réponse oestrogénique, le BPA et l’oestradiol ont une puissance et une efficacité.8Le BPA et l’oestradiol sont aussi puissants l’un que l’autre à inhiber la libération d’adinopectine d’adipocytes humains à 1nM, impliquant ensuite le BPA à des niveaux d’exposition dans la résistance à l’insuline et le syndrome métabolique.9 et que par ce mécanisme non classique de réponse oestrogénique, le BPA et l’oestradiol ont une puissance et une efficacité.8Le BPA et l’oestradiol sont aussi puissants l’un que l’autre à inhiber la libération d’adinopectine d’adipocytes humains à 1nM, impliquant ensuite le BPA à des niveaux d’exposition dans la résistance à l’insuline et le syndrome métabolique.9
Les effets du BPA sur les cellules β confirment que le BPA agit comme un puissant oestrogène par cette voie de réponse-oestrogème découverte récemment, dont l’une est aussi présent dans les tissus humains ?3 De façon importante, alors que de faibles doses de BPA et d’oestradiol stimulaient cette réponse des cellules β, des doses 100 fois plus élevées de BPA et d’oestradiol ne stimulaient pas la production d’insuline des cellules β dans le modèle souris8 ou la libération d’adiponectine des adipocytes humains.9 Les courbes de réponse aux doses biphasiques ou non monotone dans cette étude et beaucoup d’autres sur le BPA suivent une forme U inversée, ce qui représente une découverte commune pour les composés chimiques et les drogues actifs sur les sécrétions endocrines, pour lesquels des doses élevées inhibent (régulent vers le bas) le système de réponse à dose faible alors qu’il introduit un vaste tableau d’autres effets contraires par des mécanismes de réponse différents.10 Malgré des dizaines d’années d’observations publiées par des endocrinologues rapportant des courbes de réponse aux doses, non-monotones pour des composés hormonaux actifs, la supposition principale édictée par la FDA, l’Agence de Protection Environnementale, et l’Autorité Européenne de la Sécurité des Aliments pour estimer la DJA pour les composés chimiques environnementaux est toujours basée sur un concept d’abord articulé au 16è siècle : « C’est la dose qui fait le poison »11 ; i.e., les courbes de réponse à la dose sont considérées comme étant monotones pour les composés chimiques environnementaux.
La FDA et l’Agence Européenne de la Sécurité des Aliments ont choisi d’ignorer les avertissements des panels d’experts12 et d’autres agences gouvernementales,4,13 et ont continué à déclarer le BPA « sûr ».14,15 Les découvertes de Lang et al1 disant que le BPA est significativement lié aux marqueurs de sérum hépatique, comme des niveaux élevés de 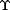 –glutamyltransférase, qui étaient prédictifs de maladie métabolique, de maladie cardiaque, et qui augmentaient la mortalité dans l’étude longitudinale de Framingham,16 défient la sécurité du BPA. Un facteur qui peut contribuer au refus des agences de régulation à entreprendre une action contre le BPA face à la preuve accablante du dommage due aux études animales rapportées dans des publications de pairs par des scientifiques académiques et gouvernementaux est une campagne agressive de désinformation utilisant des techniques (« doute manufacturé ») tout d’abord développée par le plomb, le vinyle, et les industries du tabac à défier la fiabilité des découvertes publiées par des scientifiques indépendants.17,18 –glutamyltransférase, qui étaient prédictifs de maladie métabolique, de maladie cardiaque, et qui augmentaient la mortalité dans l’étude longitudinale de Framingham,16 défient la sécurité du BPA. Un facteur qui peut contribuer au refus des agences de régulation à entreprendre une action contre le BPA face à la preuve accablante du dommage due aux études animales rapportées dans des publications de pairs par des scientifiques académiques et gouvernementaux est une campagne agressive de désinformation utilisant des techniques (« doute manufacturé ») tout d’abord développée par le plomb, le vinyle, et les industries du tabac à défier la fiabilité des découvertes publiées par des scientifiques indépendants.17,18
Par conséquent, il existe une discordance marquée entre la DJA du BPA couramment acceptée de 50µg/kg par jour et de nombreux effets indésirables chez les animaux se produisant à des niveaux très inférieurs à ce dosage dans des expérimentations récentes utilisant les outils de la biologie du 21è siècle.2 Un problème fondamental est que la DJA courante pour le BPA est basée sur des expériences menées au début des années 80 en utilisant des méthodes dépassées (seules des doses très élevées ont été testées) et des tests d’insensibilité. Des découvertes plus récentes de scientifiques indépendants ont été rejetées par la FDA, apparemment parce que ces chercheurs ne suivaient pas les directives de test dépassés pour les composés chimiques environnementaux, alors que des études utilisant les tests dépassés d’insensibilité (impliquant principalement des études financées par l’industrie chimique) ont plus de poids en arrivant à la conclusion que le BPA n’est pas dangereux à des niveaux d’exposition actuels.15
Si des adultes avec des niveaux élevés de BPA présentent un risque plus grand de maladies métaboliques, comme le suggèrent les découvertes de Lang et al,1 les études longitudinales de suivi chez les bébés, les enfants, et les adolescents, aussi bien que chez les femmes enceintes et les fœtus, présenteraient une priorité élevée pour 2 raisons. Premièrement, il existe un consensus du panel d’experts sponsorisé par les Instituts Nationaux de Santé12 d’autres rapports d’agences gouvernementales, y compris le Programme Américain National Toxicologique 13 et le Ministère de la Santé Canadien,4 qui dit que l’exposition au BPA pendant le développement pose le risque le plus important pour les effets secondaires ; on pense que le fœtus et l’enfant en bas âge sont plus susceptibles aux effets oestrogéniques du BPA du fait de la petite taille de leur corps et de leur capacité limitée à métaboliser le BPA.19 Deuxièmement, avec l’augmentation exponentielle de l’utilisation du BPA dans les objets durant les 30 dernières années, il y a eu une augmentation énorme sur l’incidence de l’obésité et le diabète de type 2 chez l’enfant.20 De très faibles doses de BPA pendant la vie fœtale/néonatale chez les rongeurs augmentent le taux de croissance postnatale aussi bien que durant la puberté avancée, avec comme suite une perturbation de la fonction neuroendocrinienne.2 Un rôle causal du BPA dans ces tendances est plausible parce que le BPA peut altérer la programmation des gênes pendant les périodes critiques de différentiation cellulaire pendant le développement fœtal et néonatal. Ce processus, mentionné comme « programmation épigénétique », peut résulter en l’expression de maladies métaboliques et de cancers dans la vie future.21,22 Examiner les effets développementaux nécessitera un biomonitoring du BPA (et d’autres composés chimiques impliquant une perturbation de la fonction endocrinienne) dans des études longitudinales qui lient des expositions pendant les périodes critiques du développement à une maladie en résultant. Cependant, de nouvelles preuves de dangerosité ne devraient pas être requises pour qu’une action de régulation débute le processus de réduction d’exposition au BPA.4
Le rapport de Lang et al1devrait stimuler des études plus approfondies et une réévaluation des suppositions de base sur les évaluations de risque qui ont conduit aux assurances que le BPA est sûr.15 Leurs découvertes intensifient aussi les motivations pour que la chimie verte (un nouveau domaine basé sur la collaboration entre biologistes et chimistes à développer des composés chimiques biologiquement inertes à utiliser dans des produits) trouve des remplaçants rentables des applications du BPA contribuant aux expositions étendues à l’homme.23 Etant donné que la production mondiale de BPA atteint maintenant 7 milliards de livres par an, 17 il sera bien plus aisé d’éliminer les expositions directes à son utilisation dans les récipients alimentaires et de boissons que de trouver des solutions à la contamination mondiale massive par ce composé chimique due à son rejet par enfouissement de déchets et le rejet dans l’écosystème aquatique de myriades d’autres produits contenant du BPA, BPA que le Canada a déjà déclaré comme étant un contaminant environnemental majeur.4
La bonne nouvelle est que l’action du gouvernement à réduire les expositions peut offrir une intervention efficace pour améliorer la santé et réduire le poids de certains des problèmes de santé humains qui ont le plus de conséquences. Ainsi, même en attendant confirmation des découvertes de Lang et al1 les prochaines étapes logiques pour réduire le risque de santé publique consiste à diminuer l’exposition au BPA et à développer des alternatives à son utilisation.
Informations sur les auteurs
 |  |
Correspondance : Frederick S. vom Saal, PhD, Division of Biological Sciences, 105 Lefevre Hall, University of Missouri, Columbia, MO 65211 (vomsaalf{at}missouri.edu).
Liens financiers : le Dr vom Saal a rapporté travaillé dans le comité organisateur de l’Institut National de Santé (NIH en américain)-qui a sponsorisé la conférence sur le bisphénol A (BPA) tenue à Chapel Hill, Caroline du Nord, en 2006 ; il a participé comme témoin expert de la défense dans un procès en 2004 concernant les effets du bisphénol sur la santé ; il a travaillé comme consultant pour la préparation d’un litige concernant le BPA ; il a travaillé comme président directeur général de LLC XenoAnalytical, qui utilise une variété de techniques analytiques pour mesurer l’activité oestrogénique et le BPA dans les tissus et les lixiviats de produits ; et il assure la maintenance d’un site Internet (http://endocrinedisruptors.missouri.edu/vomsaal/vomsaal.html) qui contient un document avec des références et des extraits d’articles publiés sur le BPA. Le Dr Myers a rapporté avoir travaillé dans le cadre du comité organisateur de la conférence sponsorisée par le NIH sur le BPA qui s’est tenue à Chapel Inn, Caroline du Nord, en 2006 ; il a travaillé en tant que président directeur général/scientifique en chef d’une organisation à but non lucratif, les Sciences de Santé Environnementale, qui rassemble et redistribue les informations sur l’environnement et la santé de sources médiatiques partout dans le monde (EnvironmentalHealthNews.org ; y est incluse la couverture du BPA lorsqu’elle existe, et aucune contribution n’est exigée pour ce service parce qu’il est soutenu financièrement par des fondations privées) ; la publication (avec 2 co-auteurs) « Notre futur volé », livre qui mentionne brièvement le BPA (le Dr Myers a reçu moins de 10 000$ en royalties pour cet ouvrage depuis sa publication) ; et la publication d’un site Web compagnon ne générant aucun revenu (OurStolenFuture.org) qui résume la science émergeante au sujet de la perturbation endocrinienne, incluant les découvertes sur le BPA.
Les éditoriaux représentent les opinions des auteurs et du JAMA mais pas ceux de l’American Medical Association.
Affiliations des auteurs : Division of Biological Sciences, University of Missouri, Columbia (Dr vom Saal); Environmental Health Sciences, Charlottesville, Virginia (Dr Myers).
Voir aussi p 1303.
BIBLIOGRAPHIE
 |  |
1. Lang IA, Galloway TS, Scarlett A, et al.. Association of urinary bisphenol A concentration with medical disorders and laboratory abnormalities in adults. JAMA.2008;300(11):1303-1310.
FREE FULL TEXT
2. Richter CA, Birnbaum LS, Farabollini F, et al.. In vivo effects of bisphenol A in laboratory rodent studies. Reprod Toxicol. 2007;24(2):199-224.
PUBMED
3. Wetherill YB, Akingbemi BT, Kanno J, et al.. In vitro molecular mechanisms of bisphenol A action. Reprod Toxicol. 2007;24(2):178-198.
PUBMED
4. Environment Canada. Draft Screening Assessment for The Challenge: Phenol, 4,4’-(1-methylethylidene)bis-(Bisphenol A). Chemical Abstracts Service Registry No. 80-05-7. Environment Canada Web site. http://www.ec.gc.ca/substances/ese/eng/challenge/batch2/batch2_80-05-7.cfm. 2008. Accessibility verified August 20, 2008.5. Vandenberg LN, Hauser R, Marcus M, Olea N, Welshons WV. Human exposure to bisphenol A (BPA). Reprod Toxicol. 2007;24(2):139-177.
PUBMED
6. Stahlhut RW, van Wijngaarden E, Dye TD, Cook S, Swan SH. Concentrations of urinary phthalate metabolites are associated with increased waist circumference and insulin resistance in adult U.S. males. Environ Health Perspect. 2007;115(6):876-882.
PUBMED
7. Bindhumol V, Chitra KC, Mathur PP. Bisphenol A induces reactive oxygen species generation in the liver of male rats. Toxicology. 2003;188(2-3):117-124.
PUBMED
8. Alonso-Magdalena P, Ropero AB, Carrera MP, et al.. Pancreatic insulin content regulation by the estrogen receptor ER alpha. PLoS ONE. 2008;3(4):e2069.
9. Hugo ER, Brandebourg TD, Woo JG, Loftus J, Alexander JW, Ben-Jonathan N. Bisphenol A at environmentally relevant doses inhibits adiponectin release from human adipose tissue explants and adipocytes [published online August 14, 2008]. Environ Health Perspect. doi:10.1289/ehp.11537.10. Welshons WV, Nagel SC, vom Saal FS. Large effects from small exposures, III: endocrine mechanisms mediating effects of bisphenol A at levels of human exposure. Endocrinology. 2006;147(6)(suppl):S56-S69.
PUBMED
11. Trautmann N.. The dose makes the poison—or does it? ActionBioscience.org Web site. http://www.actionbioscience.org/environment/trautmann.html. 2005. Accessed August 7, 2008.12. vom Saal FS, Akingbemi BT, Belcher SM, et al.. Chapel Hill bisphenol A expert panel consensus statement: integration of mechanisms, effects in animals and potential to impact human health at current levels of exposure. Reprod Toxicol. 2007;24(2):131-138.
PUBMED
13. National Toxicology Program (NTP). Draft NTP brief on bisphenol A. NTP Web site. http://cerhr.niehs.nih.gov/chemicals/bisphenol/BPADraftBriefVF_04_14_08.pdf. April 14, 2008. Accessed July 5, 2008.14. European Food Safety Authority. Opinion of the Scientific Panel on Food Additives, Flavourings, Processing Aids and Materials in Contact with Food on a request from the Commission related to 2,2-BIS(4-HYDROXYPHENYL)PROPANE (Bisphenol A). EFSA J. 2006;428:1-76.15. Statement of Norris Alderson. PhD, Associate Commissioner for Science, Food and Drug Administration, Department of Health and Human Services, before the Subcommittee on Commerce, Trade and Consumer Protection, Committee on Energy and Commerce, US House of Representatives. US Food and Drug Administration Web site. http://www.fda.gov/ola/2008/BPA061008.html. June 10, 2008. Accessed August 12, 2008.16. Lee DS, Evans JC, Robins SJ, et al.. Gamma glutamyl transferase and metabolic syndrome, cardiovascular disease, and mortality risk: the Framingham Heart Study. Arterioscler Thromb Vasc Biol. 2007;27(1):127-133.
FREE FULL TEXT
17. vom Saal FS, Hughes C. An extensive new literature concerning low-dose effects of bisphenol A shows the need for a new risk assessment. Environ Health Perspect. 2005;113(8):926-933.
PUBMED
18. Michaels D.. Doubt Is Their Product: How Industry’s Assault on Science Threatens Your Health. New York, NY: Oxford University Press; 2008.19. Taylor JA, Welshons WV, vom Saal FS. No effect of route of exposure (oral; subcutaneous injection) on plasma bisphenol A throughout 24 hr after administration in neonatal female mice. Reprod Toxicol. 2008;25(2):169-176.
PUBMED
20. De Ferranti SD, Osganian SK. Epidemiology of paediatric metabolic syndrome and type 2 diabetes mellitus. Diab Vasc Dis Res. 2007;4(4):285-296.
FREE FULL TEXT
21. Newbold RR, Padilla-Banks E, Jefferson WN, Heindel JJ. Effects of endocrine disruptors on obesity. Int J Androl. 2008;31(2):201-208.
PUBMED
22. Prins GS, Birch L, Tang WY, Ho SM. Developmental estrogen exposures predispose to prostate carcinogenesis with aging. Reprod Toxicol. 2007;23(3):374-382.
PUBMED
23. Anastas PT, Beach ES. Green chemistry: the emergence of a transformative framework. Green Chem Let Rev. 2007;1(1):9-24.
ARTICLES EN RAPPORT
Cette semaine dans le JAMA-Français
JAMA. 2008;300:1273.
Texte Complet
Le statut dans la santé des adultes du taux de bisphénolurinaire
Iain A. Lang, Tamara S. Galloway, Alan Scarlett, William E. Henley, Michael Depledge, Robert B. Wallace, et David Melzer
JAMA. 2008;300:1303-1310.
Résumé
| Texte Complet
|